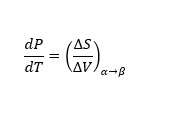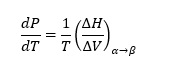Équilibre De Phase
L’ÉQUILIBRE DE PHASE EST L’ÉTUDE DE L’ÉQUILIBRE EXISTANT ENTRE OU AU SEIN DE DIFFÉRENTS ÉTATS DE MATIÈRE, À SAVOIR SOLIDE, LIQUIDE ET GAZEUX. L’ÉQUILIBRE EST DÉFINI COMME UNE ÉTAPE QUAND LE POTENTIEL CHIMIQUE DE TOUT ÉLÉMENT PRÉSENT DANS LE SYSTÈME RESTE STABLE AU FIL DU TEMPS. LA PHASE EST UNE RÉGION DANS LAQUELLE L’INTERACTION INTERMOLECULAIRE EST SPATIALEMENT UNIFORME OU, EN D’AUTRES TERMES, LES PROPRIÉTÉS PHYSIQUES ET CHIMIQUES DU SYSTÈME SONT LES MÊMES DANS TOUTE LA RÉGION. AU SEIN DU MÊME ÉTAT, UN COMPOSANT PEUT EXISTER EN DEUX PHASES DIFFÉRENTES, COMME LES ALLOTROPES D’UN ÉLÉMENT. EN OUTRE, DEUX COMPOSÉS IMMISCIBLES DANS LE MÊME ÉTAT LIQUIDE PEUVENT COEXISTER DANS DEUX PHASES.
L’équilibre de phase a de nombreuses applications dans les industries, y compris la production de différents allotropes de carbone, l’abaissement du point de congélation de l’eau par dissolution du sel (saumure), la purification de composants par distillation, l’utilisation d’émulsions dans la production alimentaire, l’industrie pharmaceutique, etc. L’équilibre de phase solide-solide occupe une place particulière dans la métallurgie et sert à la fabrication d’alliages de propriétés physiques et chimiques différentes. Par exemple, le point de fusion des alliages de cuivre et d’argent est inférieur au point de fusion du cuivre ou de l’argent.
Diagrammes de phase
Les diagrammes de phases sont utilisés pour comprendre la relation entre différentes phases, et sont généralement représentés comme le changement dans la phase d’un système en fonction de la température, de la pression ou de la composition des composants dans un système. Le système existe dans une phase où l’énergie libre de Gibbs du système est minimale. À l’équilibre, la température, la pression et le potentiel chimique des molécules à composant constitutif dans le système doivent être identiques pendant toutes les phases. La figure 1 présente un schéma général du diagramme de phase d’un système à composant unique (Lue, 2009).
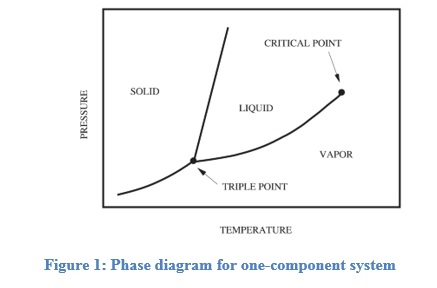
Les courbes illustrées dans la figure représentent la coexistence de deux phases. La courbe de fusion est la courbe du diagramme de phases le long de laquelle les phases solide et liquide d’un système restent en équilibre. Les phases liquide et gazeuse d’un système restent en équilibre le long de la courbe de vaporisation, tandis que la courbe de sublimation représente le stade d’équilibre entre la phase solide et la phase gazeuse. Le point triple est le point sur le graphique où coexistent les trois états, et est unique pour chaque composant. Si α et β sont deux phases quelconques dans lesquelles un composant peut exister, en utilisant la première et la deuxième loi de la thermodynamique, l’inclinaison de l’une des courbes de la figure 1 peut être représentée par
où P et T sont la pression et la température du composant, respectivement. ΔS et ΔV sont les changements d’entropie molaire et de volume molaire, respectivement, du composant lorsqu’il change sa phase de α à β en équilibre.
L’équation (1) peut également s’écrire comme
et est appelée l’équation de Clausius Clapeyron. La pression de vapeur en équilibre signifie que le nombre de molécules s’évaporant est égal au nombre de molécules se condensant à la surface de l’eau. Selon la règle de phase de Gibbs sur les systèmes à plusieurs composants, le nombre de degrés de liberté intensifs dans un système à plusieurs composants non réactif, F en équilibre, est donné par![]() (3)
(3)
où C est le nombre de composants non réactifs dans un système et n le nombre de phases. Par exemple, pour les systèmes à deux composants et à deux phases, il existe deux degrés de liberté intensifs, à savoir la température, la pression ou la fraction molaire. En d’autres termes, dans le cas d’un système à deux composants et à deux phases en équilibre, seules deux variables intensives sont nécessaires pour déterminer de manière unique l’état thermodynamique du système.
Différents types d’équilibre sont étudiés en détail, à savoir l’équilibre liquide-vapeur, l’équilibre liquide-liquide, l’équilibre solide-liquide, l’équilibre solide-solide (alliages ou formes allotropiques), etc. L’augmentation du nombre de composants, les réactions chimiques, la présence de tensioactifs et la déviation du comportement idéal font partie des causes de la complexité accrue des diagrammes de phases. Ici, nous avons discuté d’un cas particulier d’équilibre vapeur-liquide, qui est couramment utilisé dans les distilleries, à savoir les mélanges d’éthanol et d’eau.
Équilibre vapeur-liquide
La loi de Raoult stipule que la pression de vapeur partielle exercée par un composant dans une solution idéale est le produit de sa fraction molaire et de la pression de vapeur du composant pur. Ainsi, la pression de vapeur totale exercée par une solution idéale avec k composants, P est donnée par
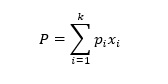 (4)
(4)
où pi est la pression de vapeur du composant pur et xi est la fraction molaire respective. Par exemple, si dans une solution hypersaline (mélange à deux composants), un composant (sel ordinaire) a une vapeur négligeable à la température, la pression de vapeur du mélange est donc simplement le produit de la fraction molaire d’eau et de la pression de vapeur de l’eau à la température spécifiée. La loi de Raoult n’est valable que pour les solutions idéales qui ne supposent aucune interaction intermoléculaire entre différents composants, alors que dans la plupart des cas traités dans les industries, il n’existe guère de solutions idéales. La loi de Raoult modifiée est utilisée pour les solutions non idéales (J.M. Smith, 2005) ; en conséquence, la pression totale exercée, P est exprimée par
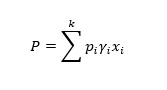 (5)
(5)
où yi est le coefficient d’activité du ieme composant.
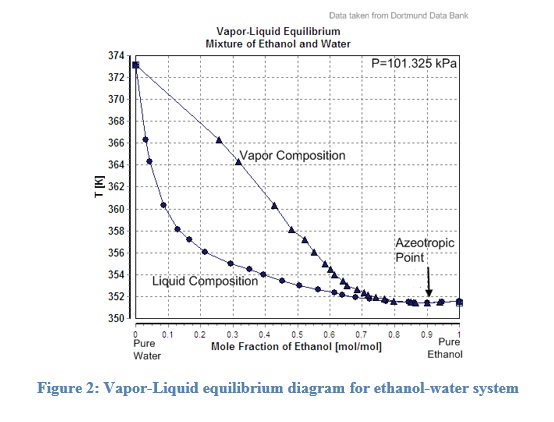
Figure 2 : Diagramme d’équilibre vapeur-liquide pour système éthanol-eau
La figure 2 montre le diagramme de phase des mélanges d’éthanol et d’eau (Banque de données de Dortmund). Des graphiques similaires sont utilisés dans les distilleries pour calculer les températures souhaitées pour des compositions de sortie spécifiques. Il contient une courbe de vapeur et une courbe de liquide permettant d’estimer les compositions de vapeur ou de liquide. La courbe de vapeur est également appelée courbe de point de rosée, tandis que la courbe de liquide se dénomme aussi courbe de point d’ébullition. Fait intéressant, les courbes se rejoignent à leur point le plus bas, ce qui suggère que si un mélange d’éthanol et d’eau est encore bouilli, il aura la même composition en phase vapeur. Par conséquent, la concentration maximale en éthanol obtenue par simple procédé de distillation dans un mélange d’éthanol et d’eau serait de 95,5%. Ces mélanges qui ont le point d’ébullition le plus bas/le plus haut sur le diagramme de phases et ne peuvent pas être purifiés davantage sont appelés Azéotropes. Les azéotropes présentent un point d’ébullition plus élevé ou plus bas que l’un ou l’autre de leurs éléments constitutifs, selon que les mélanges présentent des écarts positifs ou négatifs par rapport à la loi de Roult, respectivement. Dans le cas de systèmes à trois composantes ou à trois phases, des graphes triangulaires sont utilisés avec trois extrémités de triangle représentant les trois composantes pures (phases).
Références
Dortmund Data Bank.
J.M. Smith, H. V. (2005). Introduction to Chemical Engineering Thermodynamics. New York: McGraw Hill.
Lue, L. (2009). Chemical Thermodynamics. Leo Lue & Ventus publishing APS.